Exercícios sobre a ligação dos metais
Nas siderúrgicas é feita a produção de ferro por meio do mineral hematita (Fe2O3), que passa por reações de oxirredução em altos-fornos. O ferro é bastante usado em nosso cotidiano, principalmente na produção de ligas metálicas, tais como o aço comum e o aço inoxidável. As ligações químicas que mantêm os átomos de ferro que são produzidos nas siderúrgicas são do tipo:
-
Iônica.
-
Covalente
-
Dipolo-dipolo.
-
Metálica.
-
Cristalina.
Alternativa “d”.
Quando se entra em uma sauna com corrente de ouro no pescoço, tem-se, pouco tempo depois, uma sensação de acentuado aquecimento nessa região do corpo. O fenômeno ocorre como consequência da:
-
Temperatura mais elevada da pele.
-
Ligação metálica da corrente de ouro.
-
Transferência de calor do metal para a pele.
-
Transferência de elétrons da pele para o metal.
-
Transferência de calor da pele para o metal.
Alternativa “c”.
Os metais são bons condutores de eletricidade e de calor.
(UFMG) Nas figuras I e II, estão representados dois sólidos cristalinos, sem defeitos, que exibem dois tipos diferentes de ligação química:
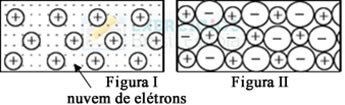
Considerando-se essas informações, é correto afirmar que:
a) a Figura II corresponde a um sólido condutor de eletricidade.
b) a Figura I corresponde a um sólido condutor de eletricidade.
c) a Figura I corresponde a um material que, no estado líquido, é um isolante elétrico.
d) a Figura II corresponde a um material que, no estado líquido, é um isolante elétrico.
Alternativa “b”.
- Errada. A figura II trata-se de um retículo cristalino formado por ligações iônicas, como o sal (NaCℓ), que só conduz eletricidade no estado fundido ou em meio aquoso.
- Correta. A figura I corresponde a uma ligação metálica, e todos os metais são sólidos condutores de eletricidade.
- Errada. Conforme dito na letra “a”, no estado líquido (fundido), ele não é isolante, mas conduz eletricidade.
- Errada. Os metais também conduzem corrente elétrica no estado líquido.
(UFC-CE) Nenhuma teoria convencional de ligação química é capaz de justificar as propriedades dos compostos metálicos. Investigações indicam que os sólidos metálicos são compostos de um arranjo regular de íons positivos, no qual os elétrons das ligações estão apenas parcialmente localizados. Isto significa dizer que se tem um arranjo de íons metálicos distribuídos em um “mar” de elétrons móveis. Com base nessas informações, é correto afirmar que os metais, geralmente:
-
têm elevada condutividade elétrica e baixa condutividade térmica.
-
são solúveis em solventes apolares e possuem baixas condutividades térmica e elétrica.
-
são insolúveis em água e possuem baixa condutividade elétrica.
-
conduzem com facilidade a corrente elétrica e são solúveis em água.
-
possuem elevadas condutividades elétrica e térmica.
Alternativa “e”.






