Exercícios sobre Número Atômico e Número de Massa
Qual o número de massa (A) de um átomo de cálcio (Z = 20) com 20 nêutrons?
A = Z + n
A = 20 + 20
A = 40
O número atômico (Z) e o número de massa (A) de um íon monoatômico com carga 3+ que contém 10 elétrons e 14 nêutrons são, respectivamente:
a) 13, 27
b) 24, 21
c) 14, 24
d) 13, 24
e) 14, 27
Alternativa correta é a letra “a”
Podemos representar o íon monoatômico com carga 3+ por: X3+.
Esse íon é constituído por 10 elétrons e 14 nêutrons. O fato de esse íon apresentar a carga +3 indica que o átomo no estado fundamental perdeu 3 elétrons, assim seu número de prótons (número atômico (Z) ) é 3 unidades maior que o seu número de elétrons:
e- = 10 → Z = e- +3 → Z = 10 +3 → Z =13
Já o número de massa é obtido somando-se o número de prótons com o número de nêutrons:
A = Z + n →A = 13 + 14 → A = 27
(UFG – GO) O número de prótons, nêutrons e elétrons representados por 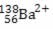 é, respectivamente:
é, respectivamente:
a) 56, 82 e 56
b) 56, 82 e 54
c) 56, 82 e 58
d) 82, 138 e 56
e) 82, 194 e 56
Alternativa “b”
A representação de um elemento químico é dada colocando-se o número atômico (Z) ou número de prótons (p) na parte inferior esquerda. Já o número de massa (A) fica na parte superior e do outro lado está escrita a carga, indicando quantos elétrons o átomo perdeu ou ganhou.
ZXA ou AzX
p = Z → p = 56
n = A – p → n = 138-56 → n = 82
Já o número de elétrons é dado pelo número de prótons menos 2 (pois a carga indica que ele perdeu dois elétrons):
e = 56-2 → e = 54
(Unifor – CE) Dentre as espécies químicas:
5B9 5B10 5B11 6C10 6C12 6C14
as que representam átomos cujos núcleos possuem 6 nêutrons são:
a) 6C10 6C12
b) 5B11 6C12
c) 5B10 5B11
d) 5B9 6C14
e) 5B10 6C14
Alternativa “b”
Para saber a quantidade de nêutrons que há em cada um dos núcleos dos átomos, basta diminuir o número de massa (A) que fica na parte superior, pelo número atômico (Z), que fica na parte inferior:
5B9 → 9 - 5 = 4
5B10 → 10 - 5 = 5
5B11 → 11 - 5 = 6
6C10 → 10 - 6 = 4
6C12 → 12 - 6 = 6
6C14 → 14 - 6 = 8
Assim, os únicos que possuem 6 nêutrons no núcleo são 5B11 e 6C12






