Exercícios sobre Titulação
Qual dos indicadores abaixo é o mais apropriado para ser usado na titulação de uma solução de ácido acético (ácido fraco) 0,20 mol . L-1 com uma solução de NaOH 0,20 mol . L-1?
-
Alaranjado-de-metila (intervalo de mudança de cor: 3,1 a 4,4).
-
Tornassol azul (intervalo de mudança de cor: 1,0 a 6,9).
-
Azul-de-bromotimol (intervalo de mudança de cor: 1,2 a 2,8).
-
Fenolftaleína (intervalo de mudança de cor: 8,2 a 10).
Alternativa “d”.
Visto que nesse caso o ponto de viragem (mudança de cor) ocorre em pH básico (valores acima de 7,0), a fenolftaleína é a mais indicada, pois a sua mudança de cor está compreendida também em um intervalo de pH básico. Por outro lado, todos os outros indicadores têm o seu ponto de viragem envolvendo pH ácido (valores abaixo de 7,0).
Considere um indicador ácido-base que adquire a cor amarela em meio ácido e azul em meio básico, como esquematizado na figura abaixo:
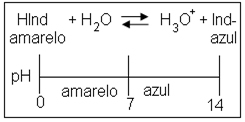
Indique a afirmativa que alista as cores apresentadas pelo indicador considerado adicionado às soluções de hidróxido de cálcio, ácido nítrico, ácido acético, hidróxido de amônio e água:
-
Amarelo, azul, azul, amarelo e amarelo.
-
Azul, verde, verde, azul e amarelo.
-
Azul, amarelo, amarelo, azul e verde.
-
Verde, amarelo, verde, azul e verde.
-
Azul, amarelo, verde, verde e verde.
Alternativa “c”.
- Hidróxido de cálcio: meio básico, pH > 7 (azul)
- Ácido nítrico: meio ácido, pH < 7 (amarelo)
- Ácido acético: meio ácido, pH < 7 (amarelo)
- Hidróxido de amônio: meio básico, pH > 7 (azul)
- Água: meio neutro, pH = 7 (verde).
(FCC) Dois equipamentos de laboratório comumente utilizados em titulações são:
-
Funil de separação e bureta.
-
Bureta e erlenmeyer.
-
Balão de fundo redondo e condensador.
-
Balão volumétrico e cadinho.
-
Pipeta e mufla.
Alternativa “b”.
Na titulação, coloca-se um volume conhecido da solução-problema, isto é, da solução que desejamos descobrir a concentração em mol/L (solução denominada de titulado), e em uma bureta, coloca-se a solução a qual se sabe a concentração, que é denominada de titulante.
(FCMSC-SP) Em titulação, a solução que está sendo titulada, em geral, está contida em um:
-
Cadinho.
-
Bureta.
-
Erlenmeyer.
-
Condensador.
Alternativa “c”.






