Exercícios sobre mudanças de estado físico
Esta lista de exercícios contempla as mudanças de estado físico da matéria bem como a análise de curvas de aquecimento e tabelas.
Publicado por: Stéfano Araújo NovaisQuestões
-
Questão 1
(EAM/2022) O derretimento de um pedaço de ferro seria um exemplo de um fenômeno denominado:
a) solidificação.
b) fusão.
c) vaporização.
d) sublimação.
e) condensação.
Letra B.
O derretimento é a transformação de algo no estado sólido para o estado líquido; portanto, é uma fusão.
-
Questão 2
(UFV/2022) Recentemente, astrônomos fizeram uma descoberta interessante a respeito de uma das luas do quinto planeta do Sistema Solar, o planeta Júpiter. Leia o fragmento da reportagem a seguir. O conhecimento de Júpiter é fundamental para a compreensão de como os planetas gigantes gasosos e seus satélites se formam e evoluem. Astrônomos detectaram, pela primeira vez, evidências de vapor d’água na atmosfera de Ganimedes, a lua de Júpiter, considerada a maior do sistema solar. O vapor d’água se forma quando o gelo da superfície da lua passa de sólido a gasoso. A descoberta foi publicada na revista Nature Astronomy.
(ROCHA, Lucas. Hubble detecta vapor de água na atmosfera de Ganimedes, lua de Júpiter. CNN Brasil. Disponível em: <https://www.cnnbrasil.com.br/tecnologia/hubbledetecta-vapor-de-agua-na-atmosfera-de-ganimedes-lua-de-jupiter/> . Acesso em: 01 set. 2021.)
Considerando o trecho sublinhado da reportagem acima, pode-se concluir que a mudança de estado físico sofrida e a condição para que ela ocorra é a:
a) condensação, com respectiva liberação de calor.
b) vaporização, com respectiva absorção de calor.
c) solidificação, com respectiva liberação de calor.
d) sublimação, com respectiva absorção de calor.
Letra D.
O trecho sublinhado cita uma passagem direta do gelo da superfície da Lua, no estado sólido, para o estado vapor, sem a passagem pelo estado líquido. Isso configura um processo de sublimação, nesse caso, com absorção de calor, uma vez que a energia deve ser absorvida para romper as interações que ocorrem entre as partículas do sólido.
-
Questão 3
(CEFSA/2022.2) A cidade de Doha, no Catar, é uma das localidades da Ásia que apresenta as maiores diferenças de temperaturas ao longo do ano. Nos meses de inverno, a temperatura mínima atinge 13 ºC e, nos meses de verão, a temperatura máxima atinge 41 ºC.
(https://pt.climate-data.org. Adaptado.)
Considere os dados das substâncias numeradas de 1 a 5.
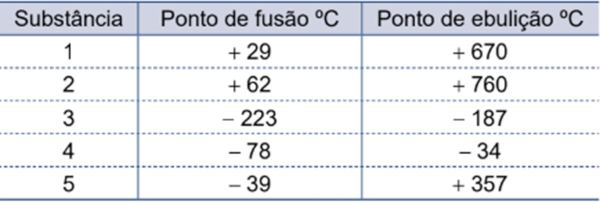
Mantendo-se essas substâncias em um ambiente sob as mesmas condições de variação de temperatura da cidade de Doha, como descrito no texto, a substância que mudará de estado físico ao longo do ano é a de número
a) 1.
b) 2.
c) 3.
d) 4.
e) 5.
Letra A.
Na cidade de Doha, a temperatura mínima é de 13 °C, enquanto a máxima atinge os 41 °C. A substância I apresenta um ponto de fusão de 29 °C, o que quer dizer que, durante as épocas de menores temperaturas, irá se apresentar no estado sólido, ao passo que, durante as épocas de maiores temperaturas, irá se apresentar no estado líquido.
-
Questão 4
(FMABC/2022) Analise o gráfico, que representa a curva de temperaturas de início de fusão de ligas cobre-níquel com diferentes composições.
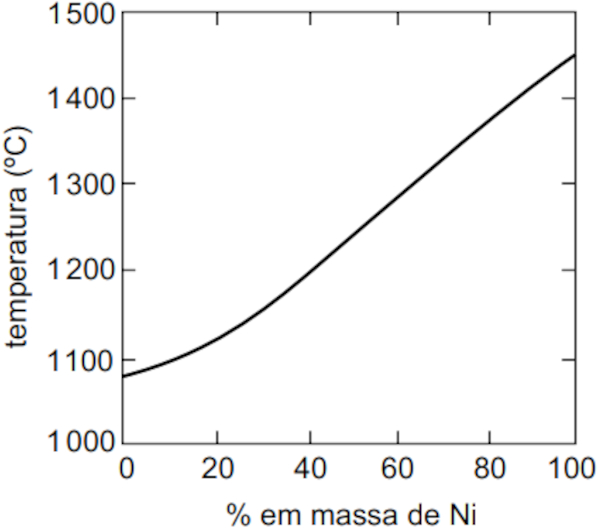
Considere as ligas que apresentam as seguintes composições, todas no estado sólido.
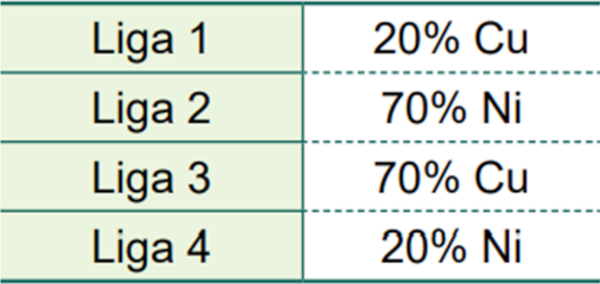
Essas quatro ligas foram aquecidas de 1000 °C até 1200 °C.
Permaneceram totalmente no estado sólido somente as ligas
a) 1 e 3.
b) 1 e 2.
c) 2 e 3.
d) 3 e 4.
e) 2 e 4.
Letra B.
A análise do gráfico demonstra que as ligas de cobre-níquel que apresentam maior temperatura de início de fusão são aquelas que apresentam maior percentual em massa de níquel e, consequentemente, menor teor de cobre. Na temperatura de 1200 °C, permanecerão sólidas as ligas que tiverem, pelo menos, 40-50% em massa de Ni, conforme observado no gráfico.
Assim sendo, as ligas que conseguirão se manter sólidas no aquecimento de 1000 °C até 1200 °C são as ligas 1 e 2, que apresentam, respectivamente 80% e 70% de Ni.
-
Questão 5
No rigoroso inverno de alguns países do Hemisfério Norte, como Rússia e Canadá, é possível ver alguns vídeos de pessoas fazendo uma brincadeira com as suas roupas que consiste em molhá-las e então deixá-las no varal por alguns minutos. Ao retornarem, percebem as peças de roupa duras como pedra, uma consequência direta das baixíssimas temperaturas.
Analisando essa situação, identifique a mudança de estado físico que ocorre durante essa brincadeira.
a) Fusão
b) Solidificação
c) Ebulição
d) Vaporização
e) Condensação
Letra B.
A roupa endurece porque a água líquida, sob baixíssimas temperaturas, acaba se solidificando, tornando-se gelo.
-
Questão 6
A produção de leite em pó envolve um processo conhecido como liofilização. Nesse processo, o leite é congelado sob baixíssimas temperaturas (por volta de -20 °C), e, então, essa amostra é levada para uma câmara de vácuo, na qual a baixa pressão faz com que a água congelada presente seja vaporizada sem a passagem pelo estado líquido. Após isso, o leite desidratado, conhecido como leite em pó, está pronto.
Na câmara de vácuo ocorre um importante processo de mudança de estado físico, que pode ser identificado como:
a) condensação
b) evaporação
c) solidificação
d) sublimação
e) fusão
Letra D.
Na câmara de vácuo, como o texto diz, a baixa pressão faz com que a água presente no leite passe diretamente do estado sólido para o estado gasoso sem a passagem pelo estado líquido, o que configura uma sublimação.
-
Questão 7
Observe a tabela a seguir, que apresenta as temperaturas de fusão e ebulição de algumas substâncias conhecidas.
Substância
T. de fusão (ºC)
T. de ebulição (ºC)
Cloro
-101
-34,6
Mercúrio
-38,3
356,6
Iodo
113,5
184
Água
0
100
Chumbo
327
1749
Nos dias mais quentes do verão brasileiro, a temperatura ambiente fica por volta dos 40 °C. Com base nessa situação e na sua análise da tabela, é possível dizer que as substâncias que estarão no estado sólido nos dias mais quentes do verão brasileiro são:
a) cloro e mercúrio.
b) iodo e água.
c) chumbo e iodo.
d) chumbo e água.
e) mercúrio e iodo.
Letra C.
Sabendo que no verão brasileiro as temperaturas ficam na faixa dos 40 °C, é possível perceber, pela análise da tabela, que apenas iodo e chumbo têm uma temperatura de fusão acima dos 40 °C, mantendo-se como sólidos nessa situação. O cloro será um gás, enquanto mercúrio e água se apresentarão no estado líquido.
-
Questão 8
Observe o gráfico a seguir, que representa o perfil de aquecimento de dois sistemas hipotéticos, A e B.
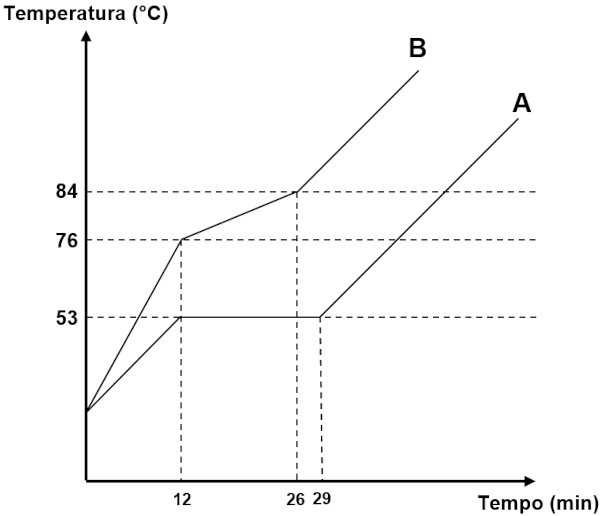
Com base na análise das curvas de aquecimento, é possível afirmar que:
a) O sistema B corresponde a uma substância pura.
b) Durante a mudança de fase, a temperatura do sistema B permanece constante.
c) A mudança de fase no sistema A tem duração de 17 minutos.
d) O sistema A apresenta variação de temperatura durante a mudança de fase.
e) A mudança de fase no sistema B demora mais tempo para ocorrer que no sistema A.
Letra C.
Observando o eixo horizontal, que corresponde ao tempo, é possível perceber que a mudança de fase no sistema A se inicia aos 12 minutos, encerrando-se aos 29 minutos. Portanto, a duração dessa mudança de fase é de 17 minutos.
-
Questão 9
O gráfico abaixo representa as mudanças de estado físico de uma substância hipotética, avaliando a temperatura (°C) com o tempo (minutos, mn):
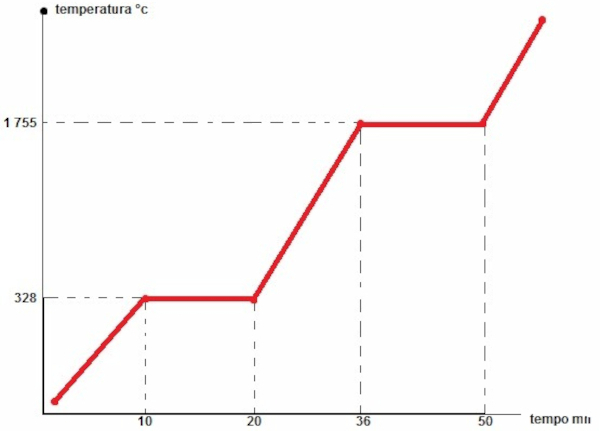
Com base na sua interpretação do gráfico, é possível afirmar que:
a) Trata-se de uma substância pura, já que as mudanças de fase ocorrem com temperatura constante.
b) A fusão da substância ocorre em 1755 °C.
c) Entre 20 e 36 minutos, a substância está sólida.
d) A ebulição ocorre mais rapidamente que a fusão.
e) A partir dos 50 °C, a substância se apresenta tanto no estado líquido quanto no estado gasoso.
Letra A.
As substâncias puras apresentam mudança de estado físico com temperatura constante, o que é observado aos 328 °C, durante a fusão, e aos 1755 °C, durante a ebulição.
-
Questão 10
É sabido, popularmente, que, depois de muitos dias de Sol, uma chuva está por vir. Isso porque o Sol tem papel crucial na formação de nuvens que farão chover sobre nós. Por meio do calor gerado por essa estrela, a água dos rios, mares, lagos e até mesmo da transpiração dos seres vivos evapora, e, nas altitudes elevadas, onde a temperatura é baixa, as nuvens se formam. Quando elas ficam cheias de água, começam a cair as primeiras gotas de chuva.
Após a leitura do texto, identifique as mudanças de estado físico presentes nele:
a) ebulição e fusão.
b) evaporação e condensação.
c) condensação e solidificação.
d) sublimação e condensação.
e) fusão e sublimação.
Letra B.
A ação do Sol sobre massas líquidas de água configura uma evaporação (uma vaporização lenta), enquanto a formação de nuvens só é possível por conta da condensação do vapor de água que ascende pela atmosfera. O acúmulo de líquido nas nuvens, portanto, permite a chuva.
-
Questão 11
Os processos envolvidos nas mudanças de estado físico da matéria, conforme figura a seguir, envolvem troca de energia na forma de calor.
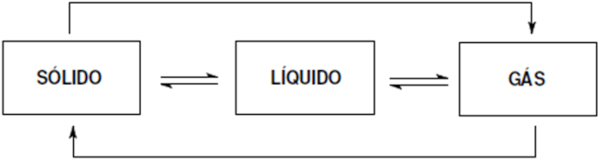
Com relação aos processos que ocorrem durante as mudanças de estado físico da matéria, um que ocorre com liberação de energia e outro, com absorção de energia, são, respectivamente:
a) solidificação e condensação.
b) fusão e vaporização.
c) solidificação e vaporização.
d) fusão e sublimação.
e) sublimação e solidificação.
Letra C.
Ocorre liberação de calor na sublimação (gás para sólido), solidificação e condensação, pois, nessas mudanças, as partículas presentes se reaproximam, aumentando seu grau de interação e perdendo energia cinética, a qual é liberada na forma de calor.
Já na fusão, vaporização e sublimação (sólido para gás), ocorre absorção de energia, uma vez que é necessário aumentar a energia cinética das partículas para romper as interações intermoleculares presentes, dando-lhes maior grau de liberdade de movimentação.
-
Questão 12
A tabela a seguir apresenta as temperaturas de fusão (T.F.) e ebulição (T.E.), em °C e a 1 atm de pressão, de cinco substâncias hipotéticas: I, II, III, IV e V.
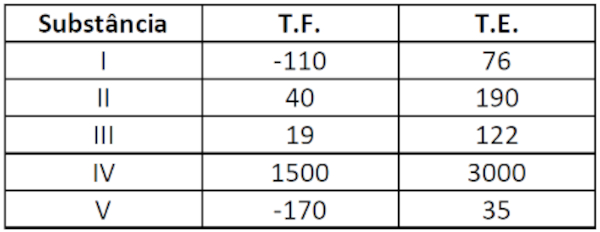
Pela análise da tabela, é possível afirmar que as substâncias líquidas na temperatura de 25 °C são:
a) I, III e V.
b) II e IV.
c) I e V.
d) II e III.
e) III e IV.
Letra A.
Para que a substância seja líquida aos 25 °C, a temperatura de fusão deve ser menor que 25 °C e a temperatura de ebulição deve ser maior que 25 °C. Nesse contexto, apenas as substâncias I, III e IV são líquidas.
A substância II é sólida, pois só sofre fusão aos 40 °C, mesmo caso da substância IV, que apenas sofre fusão na temperatura de 1500 °C.