Exercícios sobre Condições para Ocorrência de Reações
Nestes exercícios sobre condições para ocorrência de reações, é preciso pensar em fatores como afinidade, contato entre os reagentes, colisões e energia de ativação.
Publicado por: Jennifer Rocha Vargas FogaçaQuestões
-
Questão 1
(ESAL-MG) A velocidade de uma reação química depende:
I. Do número de colisões entre moléculas na unidade de tempo.
II. Da energia cinética das moléculas envolvidas na reação.
III. Da orientação das moléculas.
Estão corretas as alternativas:
a) I, II e III. b) somente I. c) somente II.
d) somente I e II. e) somente I e III.
Alternativa “a”.
-
Questão 2
(UFRGS) As figuras a seguir representam as colisões entre as moléculas reagentes de uma mesma reação em três situações:
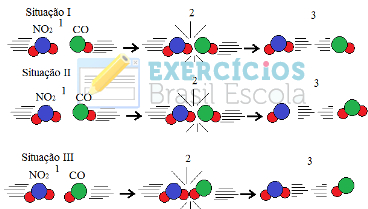
Exercício sobre colisões entre moléculas para ocorrência de reaçãoPode-se afirmar que:
a) na situação I, as moléculas reagentes apresentam energia maior que a energia de ativação, mas a geometria da colisão não favorece a formação dos produtos.
b) na situação II, ocorreu uma colisão com geometria favorável e energia suficiente para formar os produtos.
c) na situação III, as moléculas reagentes foram completamente transformadas em produtos.
d) nas situações I e III, ocorreram reações químicas, pois as colisões foram eficazes.
e) nas situações I, II e III, ocorreu a formação do complexo ativado, produzindo novas substâncias.
Alternativa “b”.
-
Questão 3
Os gases hidrogênio e oxigênio têm afinidade química para reagir. Porém, se colocarmos esses dois gases em um frasco, eles poderão ficar por tempo indeterminado lá sem que ocorra reação química. Qual fator não foi satisfeito nesse caso para a ocorrência dessa reação?
a) Afinidade química.
b) Colisões eficazes entre as partículas.
c) Contato entre os reagentes.
d) Atingir a energia de ativação.
e) Formar o complexo ativado.
Alternativa “c”.
Os gases não foram colocados em contato e, por isso, a reação não ocorreu.
-
Questão 4
Se abrirmos uma válvula de um fogareiro, ocorrendo escape de um gás inflamável, não ocorrerá nenhuma reação até que acendamos um palito de fósforo, fazendo com que ocorra uma reação de combustão entre o gás oxigênio do ar e o gás que escapou. Por outro lado, se deixarmos um giz na presença de ar, não ocorrerá nenhuma reação, mesmo que aproximemos um palito de fósforo aceso. Qual foi o fator que fez a primeira reação ocorrer e qual a condição que não foi satisfeita no segundo exemplo, resultando na não ocorrência da reação, respectivamente?
a) Contato entre os reagentes e atingir a energia de ativação.
b) Contato entre os reagentes em ambos os casos.
c) Afinidade química e atingir a energia de ativação.
d) Afinidade química em ambos os casos.
e) Atingir a energia de ativação e afinidade química.
Alternativa “e”.
No primeiro caso, a reação só ocorreu porque se acendeu o palito de fósforo e foi fornecida a energia necessária aos reagentes para que eles atingissem a energia de ativação que deu início à reação. Já no segundo exemplo, a reação não ocorreu porque não há afinidade química entre o giz e o ar, isto é, eles não possuem tendência de reagir entre si.
