Exercícios sobre moléculas
Esta lista de exercícios sobre moléculas trabalha os conceitos relacionados a essas entidades fundamentais da Química.
Publicado por: Stéfano Araújo NovaisQuestões
-
Questão 1
(UFPR – 1ª Fase/2025) Em química orgânica, o conceito de hibridação (ou hibridização) de orbitais atômicos é amplamente utilizado em função dos ângulos de ligação dos compostos de carbono. Na figura a seguir, está uma representação espacial do diclorometano (CH2Cl2) que assume uma geometria tetragonal (hibridização sp³) ao redor do átomo central, o carbono.
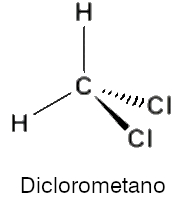
Considerando as informações apresentadas, qual é o valor de ângulo para a molécula do diclorometano, entre as ligações H-C-H, que mais se aproxima do observado experimentalmente?
A) 30º.
B) 90º.
C) 110º.
D) 180º.
E) 360º.
Letra C.
Moléculas tetraédricas apresentam um ângulo de ligação de 109,5°, aproximadamente. Isso é específico do modelo tetraédrico. Não existe geometria que coloque ângulo de 30° ou 360° para ligações químicas, enquanto 90° seria para quadrado planar e 180° para moléculas lineares.
-
Questão 2
(UFLA – PAS – 1ª Etapa/2023-2025) A polaridade de ligações e de moléculas depende da eletronegatividade e orientação dos átomos em uma molécula, e determina o modo de interação entre substâncias, como, por exemplo, entre um fármaco e uma proteína. Analise os compostos a seguir:
I. O=C=O
II. F−F
III. H−O−H
Assinale a alternativa em que o(s) composto(s) apresenta(m) ligação polar e é(são) molécula(s) polar(es).
A) Apenas I.
B) Apenas II.
C) Apenas III.
D) Apenas I e III.
Letra C.
O CO2, apesar de ligações polares, não é uma molécula polar, uma vez que a geometria linear faz com que os vetores momento dipolar das ligações C=O se anulem. Já a ligação F−F é apolar, não atendendo ao critério também.
-
Questão 3
(UFSM – Prova 1 – Tarde/2024) “Uma dieta equilibrada é tão indispensável para os nossos companheiros de quatro patas como para nós, assumindo um papel crucial no que toca a saúde, bem-estar e esperança de vida. O fornecimento adequado de todos os nutrientes vitais mantém o organismo do animal em forma, aumentando a sua imunidade e resistência e prevenindo problemas de saúde. [...] Tal como as vitaminas, os minerais são fundamentais para qualquer cão. Os minerais essenciais têm funções e propriedades muito particulares no organismo. É feita a distinção entre oligoelementos (ferro, cobre, zinco, manganês, cobalto, iodo, selênio, flúor) e macroelementos (cálcio, fósforo, magnésio, sódio, potássio).”
Fonte: ZOOPLUS MAGAZINE. Disponível em: https://www.zooplus.pt/magazine/caes/comida-para-cao/nutrientes-essenciais-para-caes. Acesso em: 05 out. 2023. (Adaptado)
Os oligoelementos e macroelementos são compostos inorgânicos que podem se ligar através de ligações iônicas ou ligações covalentes. Possuem ligações covalentes os compostos a seguir, EXCETO
A) dióxido de Selênio (SeO2 (s)).
B) nitrogênio (N2 (g)).
C) cloreto de ferro III (FeCl3 (s)).
D) oxigênio (O2 (g)).
E) flúor (F2 (g)).
Letra C.
São moléculas apenas as que possuem ligações covalentes. Para se ter uma ligação covalente, os átomos envolvidos devem ser ametais. Dessa forma, o composto C não apresenta ligação covalente (ou seja, não é uma molécula).
-
Questão 4
(UFMS – Passe – 1ª Etapa/2024-2026) Considerando os elementos químicos genéricos X (metal alcalino-terroso), Y (família do nitrogênio), W (calcogênio) e Z (halogênio), assinale a alternativa que apresenta a fórmula representativa de uma possível substância formada por dois dos elementos mencionados, cuja molécula apresente três ligações covalentes.
A) X2Z3.
B) XW2.
C) W3Z.
D) YZ3.
E) XZ2.
Letra D.
Para apresentar três ligações covalentes, o composto deve ser molecular e, assim, apresentar apenas ametais nessa constituição. Dessa forma, só pode ser formado pelos compostos Y, W ou Z.
Os halogênios possuem sete elétrons na camada de valência, precisando receber 1 elétron para estabilizar (ou seja, fazer 1 ligação covalente).
Já os calcogênios, com seis elétrons na camada de valência, precisam realizar 2 ligações covalentes para estabilizar.
Os elementos do grupo 15 (nitrogênio), com cinco elétrons na camada de valência, precisam realizar três ligações covalentes para se estabilizar.
Dessa forma, a ligação deve ocorrer entre um átomo Y e três átomos Z, ficando na forma YZ3.
-
Questão 5
O monóxido de carbono, CO, é um composto molecular e de alta toxicidade, sendo formado durante reações de combustão incompleta.
A partir das suas características, é possível dizer que o CO apresenta:
A) ligações iônicas.
B) ligações metálicas.
C) ligações covalentes.
D) ligações de hidrogênio.
E) ligações de enxofre.
Letra C.
Sendo um composto molecular, formado apenas por ametais, dentro do CO só existem ligações covalentes.
-
Questão 6
O gás ozônio é um alótropo do oxigênio, sendo uma molécula de fórmula O3. Sobre esse composto, é possível dizer que se trata de:
A) uma molécula triatômica heteronuclear.
B) uma molécula diatômica heteronuclear.
C) uma molécula monoatômica.
D) uma molécula triatômica homonuclear.
E) uma molécula poliatômica e apolar.
Letra D.
O ozônio é uma molécula triatômica pelo fato de apresentar três átomos na sua constituição. Além disso, é também homonuclear, pois é formada por um único elemento químico.
-
Questão 7
Compostos moleculares são aqueles formados apenas por átomos ligados via ligação covalente. Dessa forma, podemos dizer que uma molécula é a que possui a fórmula química:
A) Fe (s).
B) NaCl (s).
C) HCN (g).
D) He (g).
E) K2SO4 (s)
Letra C.
O composto Fe (s) se trata de um composto metálico, que não realiza ligações covalentes, mas sim metálicas. Já NaCl e K2SO4 são compostos iônicos e, portanto, formam ligações iônicas. He é um gás nobre monoatômico, não apresentando ligações covalentes.
-
Questão 8
Assinale a alternativa que apresenta uma molécula diatômica heteronuclear.
A) H2O.
B) HF.
C) KBr.
D) O2.
E) NH3.
Letra B.
KBr não é uma molécula, mas sim um composto iônico. Já O2, apesar de diatômica, é homonuclear. Tanto H2O quanto NH3 são heteronucleares, porém a água é triatômica e a amônia é tetra-atômica.
-
Questão 9
Uma molécula que adota geometria trigonal plana deve possuir número de átomos e ângulo de ligação iguais a, respectivamente:
A) 4 e 120°.
B) 4 e 60°.
C) 3 e 180°.
D) 4 e 109,5°.
E) 3 e 120°.
Letra A.
As moléculas de geometria trigonal plana são do tipo XY3, possuindo, portanto, quatro átomos. Além disso, as ligações devem apresentar a maior distância angular possível. Sendo um triângulo, esse ângulo é de 120°.
-
Questão 10
Assinale a alternativa que apresenta uma molécula de geometria linear e também pode ser considerada como polar.
A) H2O.
B) NH3.
C) CO2.
D) O3.
E) HCN.
Letra E.
São moléculas lineares apenas CO2 e HCN. Contudo, CO2 é uma molécula apolar, já que a geometria linear coloca as ligações C=O em uma distância angular de 180°, anulando o vetor momento dipolar dessas ligações e, assim, tornando-a apolar. Já no HCN, embora o ângulo das ligações também seja de 180°, as ligações são diferentes e, dessa forma, os vetores momento dipolar não se anulam, deixando-a polar.
-
Questão 11
Macromoléculas são moléculas muito grandes, formadas por centenas de átomos e com elevada massa molecular. A partir desse princípio, podemos dizer que podemos considerar como macromolécula:
A) a amônia.
B) a água.
C) a glicose.
D) o polietileno.
E) o gás hidrogênio.
Letra D.
O polietileno é um polímero, que se trata de moléculas que reúnem milhares ou dezenas de milhares de átomos. Dessa forma, é uma molécula que atende aos critérios para se considerada como uma macromolécula.
-
Questão 12
Acerca da natureza das moléculas, observe as afirmações a seguir.
I. Se uma molécula só possui ligações polares, então ela é polar.
II. Moléculas homonucleares são formadas por um único elemento químico.
III. As moléculas devem apresentar, apenas, ligações covalentes.
IV. Apenas moléculas diatômicas podem apresentar geometria linear.
Estão corretas as afirmativas:
A) I e IV.
B) II e III.
C) I, II e III.
D) II e IV.
E) III e IV.
Letra B.
Uma molécula que possua apenas ligações polares não é, necessariamente, polar. Isso pode ser visto, por exemplo, no CH4 e no BF3, que possuem ligações polares, mas são moléculas apolares.
Moléculas com mais de dois átomos podem apresentar geometria linear também, como é o caso de CO2 e HCN.