Exercícios sobre teoria cinética dos gases
Esta lista de exercícios sobre teoria cinética dos gases aborda os aspectos relacionados com a constituição, propriedades e características dos gases ideais.
Publicado por: Jennifer Rocha Vargas FogaçaQuestões
-
Questão 1
(UFPI) De acordo com a teoria cinética dos gases, é incorreto afirmar:
a) Energia cinética média é proporcional à temperatura de Kelvin.
b) As partículas estão muito unidas e têm baixa velocidade.
c) As partículas ocupam todo o volume disponível e têm movimento livre.
d) As partículas possuem alta velocidade e ocorrem choques entre elas e contra as paredes do recipiente que as contém.
e) As partículas têm movimento desordenado.
Alternativa “b”.
Segundo a teoria cinética dos gases, as partículas constituintes de um gás estão muito afastadas umas das outras e possuem um alto grau de liberdade. Por essa razão, as partículas movimentam-se de maneira contínua e desordenada, chocando-se entre elas e com as paredes do recipiente.
-
Questão 2
(UFPI) De acordo com a teoria cinética dos gases:
a) as partículas têm movimento ordenado.
b) as partículas possuem alta velocidade e os choques entre elas são inelásticos.
c) a energia cinética média é proporcional à temperatura em ºC.
d) as partículas ocupam todo o espaço disponível e têm movimento livre.
e) as partículas estão muito afastadas e têm alta velocidade.
Alternativa “d”.
As demais estão incorretas porque, segundo a teoria cinética dos gases:
a) as partículas têm movimento desordenado.
b) os choques entre as partículas são perfeitamente elásticos, ou seja, a energia mecânica total das partículas que colidem permanece inalterada, embora uma partícula possa perder energia para outra durante a colisão.
c) a energia cinética média é proporcional à temperatura na escala Kelvin.
e) as partículas estão muito unidas e têm baixa velocidade.
-
Questão 3
Qual das figuras a seguir não apresenta uma característica dos gases em consonância com a teoria do gás ideal?
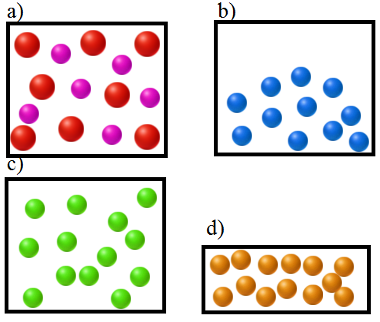
Exercício sobre gases ideaisAlternativa “b”.
A figura “b” não corresponde à característica de um gás ideal porque ele deve ocupar todo o volume do recipiente que o contém.
-
Questão 4
Avalie se são verdadeiras ou falsas as seguintes afirmações a respeito da teoria cinética dos gases ou teoria do gás ideal:
a) Quanto maior for o número de colisões de um gás com as paredes do recipiente em que está contido e entre suas partículas, maior será a pressão do gás.
b) A pressão que os gases fazem sobre a superfície da Terra é menor ao nível do mar que no alto de uma montanha.
c) Os gases apresentam volume fixo.
d) Os gases não possuem massa.
e) Quando um gás é aquecido, ele dilata-se; mas quando é resfriado, ele contrai-se.
a) Verdadeiro.
b) Falso. A pressão que os gases fazem sobre a superfície da Terra é maior ao nível do mar (pois a massa do gás é maior) que no alto de uma montanha.
c) Falso. Os gases apresentam volume variável, a depender do recipiente que o contém.
d) Falso. Qualquer gás tem massa.
e) Verdadeiro.