Exercícios sobre metais alcalinoterrosos
Nossa lista de exercícios sobre os metais alcalinoterrosos aborda todas as propriedades e particularidades dessa importante família da tabela periódica.
Publicado por: Diogo Lopes DiasQuestões
-
Questão 1
Assinale o que for correto:
a) O Ra tem maior caráter metálico que o Be.
b) O Sr tem a 1ª energia de ionização maior que o Ca.
c) Metais alcalinoterrosos possuem afinidade eletrônica maior que a dos halogênios.
d) Metais alcalinoterrosos apresentam pontos de fusão iguais aos de seus vizinhos respectivos, os metais alcalinos.
e) Possuem maior eletropositividade que os metais alcalinos.
Letra a). O caráter metálico em uma família aumenta com o aumento do número atômico. Assim, Rádio (Ra - número atômico 88) apresenta maior caráter metálico que o Berílio (Be - número atômico 4). As outras alternativas estão incorretas porque:
b – A energia de ionização na família aumenta com a diminuição do número atômico, logo, o Estrôncio (Sr - número atômico 38) tem menor energia de ionização que o Cálcio (Ca - número atômico 20);
c - A afinidade eletrônica cresce nas famílias com a diminuição do número atômico. Nos períodos, ela cresce com o aumento do número atômico. Os halogênios sempre apresentam menores e maiores valores de número atômico, respectivamente, quando comparados aos metais alcalinoterrosos, portanto, apresentam maior afinidade eletrônica;
d - O ponto de fusão de nenhum elemento é igual ao de outro;
e - Os metais alcalinos (família IA) apresentam os maiores valores de eletropositividade da tabela periódica.
-
Questão 2
Considere as afirmações sobre os elementos do grupo IIA da tabela periódica:
I- São chamados de metais alcalinoterrosos.
II- Seus raios atômicos crescem com o aumento do número atômico.
III- Seu potencial de ionização aumenta com o aumento do número atômico.
IV- Seu caráter metálico diminui com o aumento do número atômico.
São verdadeiras:
a) I e II.
b) III e IV.
c) I, II e IV.
d) II, III e IV.
e) I, II, III e IV.
Letra a). A resposta é a alternativa a porque:
I- Verdadeira.
II- Verdadeira.
III- Falsa: o potencial de ionização em uma família sempre diminui com o aumento do número atômico.
IV- Falsa: o caráter metálico em uma família sempre aumenta com o aumento do número atômico.
-
Questão 3
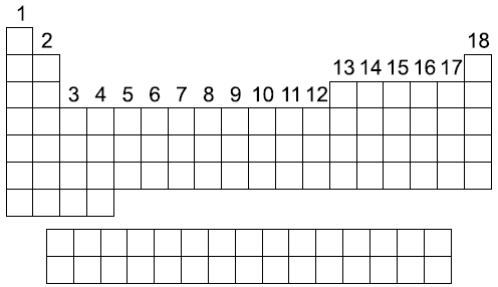
(UEL) A questão a seguir está relacionada com a representação da classificação periódica abaixo. Nessas questões, os elementos químicos estão genericamente representados por A, B, C, D, E, F, G, H, J, K, V, W, X, Y e Z.
Considere as informações a seguir sobre os elementos químicos A, B, C, D e E.
- O átomo neutro do elemento A tem 10 elétrons.
- A, B- e C+ são isoeletrônicos.
- D pertence ao 5° período e ao mesmo grupo de C, da classificação periódica.
- Entre os elementos de transição, E é o de menor número atômico.
Com base nessas informações, é INCORRETO afirmar:
a) A é um gás nobre.
b) B é um halogênio.
c) C é um metal alcalinoterroso.
d) A configuração eletrônica da camada de valência de D é 5s1.
e) E pertence ao 4° período da classificação periódica.
Letra c).
-
O elemento A, por apresentar 10 elétrons em seu átomo neutro (número de prótons igual ao número de elétrons), também apresenta 10 prótons (número atômico), o que corresponde ao gás nobre neônio (Ne);
-
A, B- (ânion monovalente, ou seja, para ter 10 elétrons, ele ganha 1 elétron) e C+ (cátion monovalente, ou seja, para ter 10 elétrons, ele perde 1 elétron) são isoeletrônicos, ou seja, apresentam o mesmo número de elétrons. Com isso, podemos afirmar que o elemento B possui número atômico igual a 9 (halogênio), e o elemento C apresenta número atômico igual a 11 (metal alcalino);
-
Se D está na mesma família do elemento C, ele também é um metal alcalino (apresenta s1 como camada de valência). Como ele está no quinto período, sua camada de valência é 5s1;
-
Metais de transição são elementos da família B (grupos 3 a 12), que se inicia no quarto período (onde estão os menores números atômicos desses elementos).
-
-
Questão 4
(PUC-Camp) Os átomos ISÓBAROS X e Y pertencem a metal alcalino e alcalinoterroso do mesmo período da classificação periódica. Sabendo-se que X é formado por 37 prótons e 51 nêutrons, pode-se afirmar que os números atômicos e de massa de Y são, respectivamente,
a) 36 e 87
b) 37 e 87
c) 38 e 87
d) 38 e 88
e) 39 e 88
Letra d). O exercício informa que o átomo X apresenta 37 prótons (que é o número atômico) e 51 nêutrons. Como X é um metal alcalino (primeira família da tabela) e Y é um metal alcalinoterroso (segunda família da tabela), o número atômico de Y é 38.
Com a soma do número de prótons com o de nêutrons de X, encontramos o seu número de massa (A):
A = próton + nêutron
A = 37 + 51
A = 88
Como os átomos X e Y são isóbaros, apresentam obrigatoriamente o mesmo número de massa. Assim, o número de massa de Y é 88.