Exercícios sobre ordem da reação
Os exercícios sobre ordem da reação mostram a relação matemática que existe entre a velocidade da reação e a concentração em quantidade de matéria dos reagentes.
Publicado por: Jennifer Rocha Vargas FogaçaQuestões
-
Questão 1
(ITA-SP) Uma certa reação química é representada pela equação:
2 A(g) + 2 B(g) → C(g)
onde A, B e C significam as espécies químicas que são colocadas para reagir. Verificou-se experimentalmente numa certa temperatura que a velocidade desta reação quadruplica com a duplicação da concentração da espécie A, mas não depende das concentrações das espécies B e C. Assinale a opção que contém, respectivamente, a expressão CORRETA da velocidade e o valor CORRETO da ordem da reação:
a) v = k [A]2 . [B]2 e 4
b) v = k [A]2 . [B]2 e 3
c) v= k [A]2 . [B]2 e 2
d) v = k [A]2 e 4
e) v = k [A]2 e 2
Alternativa “e”.
Temos a lei da velocidade genericamente como v = k [A]α . [B]β.
O enunciado diz que “ a velocidade desta reação quadruplica com a duplicação da concentração da espécie A, mas não depende das concentrações das espécies B e C.” Logo, α = 2 e β = 0. Então, temos que a lei da velocidade é dada pela seguinte expressão:
v = k [A]2. [B]0
v = k [A]2. 1
v = k [A]2
Essa reação é de segunda ordem (ou a ordem é igual a 2).
-
Questão 2
(Cefet-PR) A reação:
NO2(g) + CO(g) → CO2(g) + NO(g)
é de segunda ordem em relação ao NO2(g) e de ordem zero em relação ao CO(g). Em determinadas condições de pressão e temperatura, essa reação ocorre com velocidade v. Se triplicarmos a concentração de NO2(g) e duplicarmos a concentração de CO(g), a nova velocidade de reação v1 será igual a:
a) 3v
b) 6v
c) 9v
d) 12v
e) 18v
Alternativa “c”.
O enunciado diz que a reação é de segunda ordem em relação ao NO2(g) e de ordem zero em relação ao CO(g), o que significa que a expressão da lei da velocidade dessa reação é a seguinte:
v = k . [NO2]² . [CO]0
Se triplicarmos a concentração de NO2 e duplicarmos a concentração de CO, a equação fica assim:
v = k . [3 NO2]² . [2 CO]0
Desenvolvendo a equação, temos:
v = k . 9 . 1
v = 9 k
Ou 9v, como consta na alternativa c. -
Questão 3
Os dados da tabela abaixo se referem à reação 2 A + 3B → C.
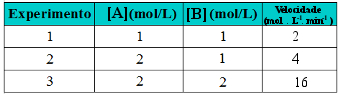
Exercício sobre ordem da reaçãoDetermine a ordem global dessa reação:
a) 1
b) 2
c) 3
d) 4
e) 5
Alternativa “c”.
Temos a lei da velocidade genericamente como v = k [A]α . [B]β.
A tabela mostra que, quando se dobrou o valor da concentração de A (experimento 1 para 2), a velocidade também dobrou. Logo, α = 1. Quando se dobrou o valor da concentração de B (experimento 1 para 3), a velocidade da reação quadruplicou. Logo, β = 2. Então, temos que a lei da velocidade é dada pela seguinte expressão:
v = k [A]1. [B]2
Somando-se esses expoentes, temos que essa reação é de terceira ordem (ou a ordem é igual a 3).
-
Questão 4
A velocidade da reação química 2 A + 3B → C + D é independente de A e fica quatro vezes maior quando dobramos a concentração de B. Determine a ordem da reação em relação a B:
a) 0
b) 1
c) 2
d) 3
e) 4
Alternativa “c”.
Se a velocidade da reação fica quatro vezes maior quando dobramos a concentração de B, então a ordem da reação em relação a B é 2.