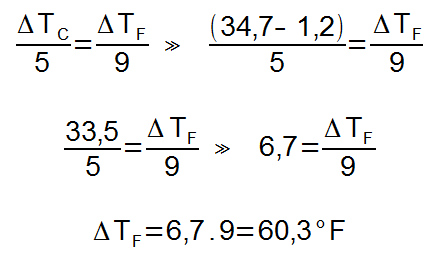Exercícios sobre Termologia
(Unirg-TO) O Brasil é reconhecidamente um país de contrastes. Entre eles, podemos apontar a variação de temperatura das capitais brasileiras. Palmas, por exemplo, atingiu, em 1º de julho de 1998, a temperatura de 13 ºC e, em 19 de setembro de 2013, a temperatura de 42 ºC (com sensação térmica de 50 ºC). Na escala Kelvin, a variação da temperatura na capital do Tocantins, entre os dois registros realizados, corresponde a:
a) 13 K
b) 29 K
c) 42 K
d) 50 K
Letra B
As escalas Celsius e Kelvin possuem 100 intervalos, desse modo, podemos concluir que as variações sofridas em ambas são iguais. Assim, podemos escrever:
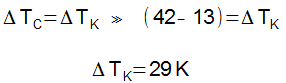
(Udesc) A queima de 1,000 g de gás de cozinha fornece 6000 cal. A massa de gás que deve ser queimada para elevar a temperatura de meio litro de água de 25,00 ºC até 100,0 ºC, e ainda produzir a evaporação de 100,0 ml de água, é:
a) 15,24 g
b) 15,23 g
c) 15,25 g
d) 15,22 g
e) 15,21 g
Letra C
Em primeiro lugar, deve-se determinar a quantidade de calor sensível necessária para elevar a temperatura da água de 25 °C para 100 °C. Adotaremos o calor específico da água como 1 cal/g°C, e meio litro de água como 500 g.
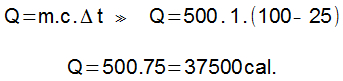
A partir da ideia de calor latente, determinaremos a quantidade de calor necessária para vaporizar 100 ml (100 g) de água. Adotaremos o calor latente de vaporização da água como 540 cal/g.
![]()
A quantidade de calor total fornecida à substância será dada pela soma das quantidades de calor determinadas acima, que resultará em 91500 cal.
Cada 1000 g de gás libera 6000 cal, logo, dividindo-se o calor total utilizado por 6000 cal, teremos a massa de gás queimada.
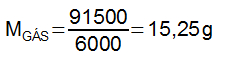
Determine a quantidade de calor necessária para levar um bloco de gelo de 1 kg de 10 °C até 5 °C.
Dados:
Calor específico do gelo = 0,5 cal/g°C
Calor latende de fusão da água = 80 cal/g
Calor específico da água = 1 cal/g°C
a) 85 kcal
b) 75 kcal
c) 100 kcal
d) 90 kcal
e) 115 kcal
Letra D
Inicialmente, deve-se elevar a temperatura do gelo até 0 °C, que corresponde ao ponto de fusão da água. Utilizaremos a massa em gramas, logo lembre-se que 1 kg = 1000 g.
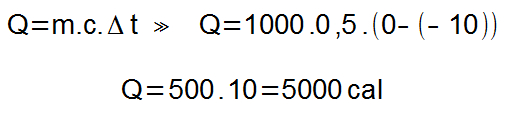
Agora, aplicaremos a equação do calor latente, para derreter completamente o bloco de gelo.
![]()
Ao derreter o gelo, obtemos água no estado líquido a 0°C. Determinaremos, então, a quantidade de calor necessária para elevar a temperatura da água de 0 °C para 5 °C.
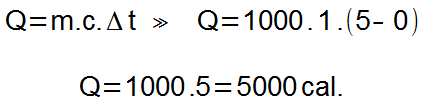
A quantidade de calor total será dada pela soma das quantidades de calor determinadas.
![]()
Em 2016, os termômetros da cidade de Goiânia indicaram 34,7 °C, maior temperatura registrada desde 1961. No ano de 1938, a cidade registrou 1,2 °C, a menor registrada na história da cidade. Determine a variação entre as temperaturas máxima e mínima, em °F, registradas em Goiânia.
a) 55,8
b) 60,3
c) 75,0
d) 30,5
e) 33,5
Letra B
Para determinar a variação de temperatura na escala Fahrenheit, basta utilizar a equação relativa às variações de temperatura.